(em atualização, favor retornar em alguns dias)
A hipertensão portal é uma condição clínica em que a pressão no sistema de veias que drenam o sangue do trato gastrointestinal para o fígado (sistema porta) aumenta. A hipertensão portal é uma condição séria e pode levar a complicações graves, incluindo ascite (acúmulo de líquido no abdômen), varizes esofágicas (veias dilatadas no esôfago), sangramento gastrointestinal e insuficiência hepática.
HIPERTENSÃO PORTAL
Pense em tudo o que você comeu no último dia. Mesmo que sua dieta seja muito boa, apenas parte dos alimentos é diretamente aproveitável pelo organismo. Alguns nutrientes precisam ser transformados antes de se tornarem úteis, as bactérias que ultrapassam a barreira do intestino precisam ser destruídas e as toxinas precisam ser inativadas antes de se espalharem pelo organismo! E o fígado é responsável por tudo isso!

Para que o fígado cumpra essas funções, ele tem uma posição muito particular no sistema circulatório: ao invés de receber o sangue arterial, rico em oxigênio e sob alta pressão vindo direto do sangue, ele recebe o sangue que já passou pelo sistema digestivo e o baço. Assim, parte do oxigênio já foi gasto para nutrir esses órgãos e a pressão que empurra esse sangue já é muito mais baixa. Para dar conta do serviço, o fígado recebe uma suplementação de oxigênio através da artéria hepática, mas a maioria do sangue que entra no fígado é o sangue venoso, rico em nutrientes (e toxinas) que se junta a partir do sistema digestivo e o baço em uma veia única, a veia porta.

A maior parte do sangue que chega ao fígado vem da veia porta, que é um sangue venoso (em azul, com baixo teor de oxigênio e de baixa pressão mas rico em nutrientes pois vem direto do sistema digestivo). A artéria hepática suplementa a necessidade de oxigênio, trazendo sangue arterial (em vermelho).
Se o fígado está bom, o sangue flui sem dificuldades pelo órgão e chega ao coração, de onde é distribuído pelo resto do corpo. Ao passar pelo fígado, os nutrientes são transformados para o uso e as toxinas são inativadas e encaminhadas para eliminação (pelo sangue, para os rins ou pela bile, para o intestino). Mas se os vasos sanguíneos estão estreitados e tortuosos, como ocorre na cirrose, o sangue não fui com a mesma facilidade e a pressão dentro da veia porta começa a aumentar. E isso leva à dilatação da veia porta, assim como de todas as veias que desembocam nela: em especial as veias que vem do estômago e do esôfago, levando à formação de varizes esofágicas e gástricas, a veia que vem do baço, levando a esplenomegalia e hiperesplenismo e as veias do peritônio, levando a ascite. Indiretamente, a dilatação de todos esses vasos provocam alterações na circulação que podem afetar até os rins (levando à chamada síndrome hepatorrenal) e os pulmões (síndrome hepatopulmonar).
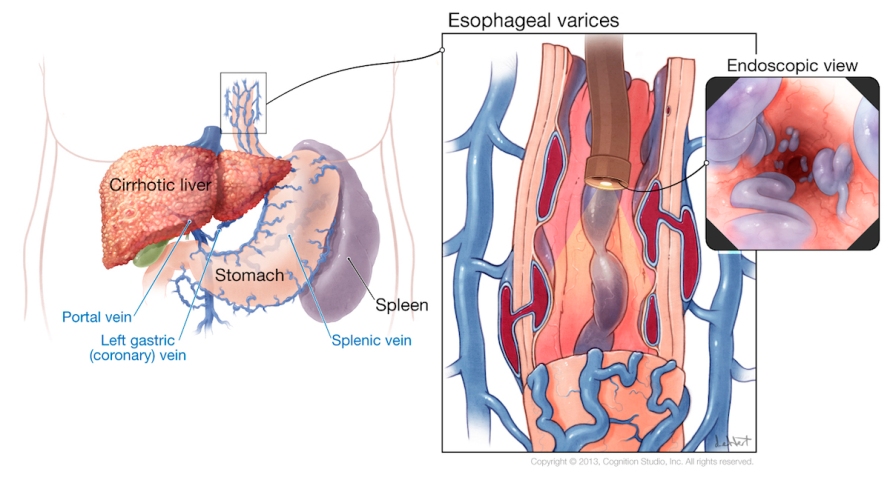
A hipertensão portal é geralmente causada por obstruções no fluxo de sangue na veia porta ou nas veias que a drenam. Estas obstruções podem ser causadas por doenças hepáticas, como cirrose ou esquistossomose, ou doenças sistêmicas, como trombose (coágulos de sangue) ou tumores. Além disso, a hipertensão portal pode ser causada por problemas na circulação do sangue nas veias, como insuficiência cardíaca ou pressão arterial elevada.
Os sintomas da hipertensão portal podem incluir inchaço abdominal, fadiga, perda de peso, náusea e vômito. No entanto, muitas vezes não há sintomas evidentes na fase inicial da doença, e a hipertensão portal é detectada apenas em exames de rotina ou em exames para outras condições médicas.
O diagnóstico da hipertensão portal é feito com base em exames de sangue, imagem (como ultrassonografia, tomografia computadorizada ou ressonância magnética) e, às vezes, angiografia (exame que usa contraste e imagem para visualizar as artérias e veias). Estes exames ajudam a identificar a causa subjacente da hipertensão portal e a avaliar a gravidade da doença.
O tratamento da hipertensão portal depende da causa subjacente e da gravidade da doença. O tratamento pode incluir medicações para controlar a pressão portal, como diuréticos ou vasodilatadores, cirurgia para corrigir obstruções no fluxo de sangue ou para desviar sangue do sistema porta. Outra estratégia é construir um shunt (“curto circuito”) do sistema porta para a veia cava inferior através do procedimento endovascular chamado de TIPS (transjugular intrahepatic portocaval shunt). Além disso, o tratamento da doença subjacente, como cirrose ou insuficiência cardíaca, também pode ajudar a controlar a hipertensão portal.
Em resumo, a hipertensão portal é uma condição séria da circulação do sangue nas veias que drenam o sangue do trato gastrointestinal para o fígado. A hipertensão portal pode ser causada por obstruções no fluxo de sangue, doenças hepáticas ou sistêmicas e problemas na circulação do sangue. Os sintomas podem incluir inchaço abdominal, fadiga, perda de peso, náusea e vômito, mas muitas vezes não há sintomas evidentes. O diagnóstico é feito com base em exames de sangue, imagem e, às vezes, angiografia. O tratamento depende da causa subjacente e da gravidade da doença e pode incluir medicações, cirurgia, radiologia intervencionista ou tratamento da doença subjacente. É importante que a hipertensão portal seja detectada e tratada o mais cedo possível para prevenir complicações graves.
Artigo elaborado em 22/05/23
Última atualização: 22/05/23

